Elektrohemijske reakcije
Elektrohemijske reakcij su reakcije kod kojih se procesi oksidacije i redukcije odvijaju u odvojenim prostorima (polućelijama) koji su međusobno povezani odgovarajućim provodnikom.
Elektrohemijska ćelija - sistem koji se sastoji od polućelija.
Postoje dva tipa:
1. Galvanska ćelija - odvijaju se spontani redoks procesi koji omogućavaju kontinuirani tok elektrona kroz provodnik, pri čemu se hemijska energija pretvara u električnu.
2. Elektrolitičke ćelije - u njima se odvijaju redoks reakcije pod dejstvom spoljašnjeg izvora električne struje pri čemu se električna energija pretvara u hemijsku energiju. To su nespontane redoks reakcije.
Galvanska ćelija
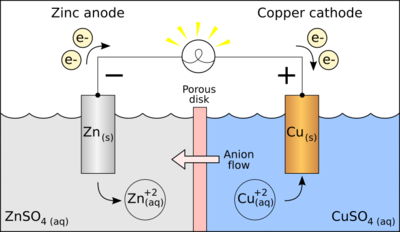
U jedan sud sa rastvorom neke soli cinka (
ZnSO4) uroni se pločica elementarnog cinka (Zn), a u drugi sud sa rastvorom soli bakra (CuSO4) uroni se pločica elementarnog bakra (Cu). Sa površine pločice cinka odvajaju se
Zn2+i prelaze u rastvor, a elektroni (e-) ostaju na pločici. Rastvor se naelektriše pozitivno (+) a pločica cinka negativno (-). U drugom sudu, elektroni sa pločice bakra prelaze na
-->Cu2+ jone (koji se nalaze u rastvoru) što dovodi do razdvajanja elementarnog bakra. Rastvor se naelektriše negativno (-), a pločica pozitivno (+).
Mehanizam se prikazuje shematski, tzv. ćelijskim dijagramom. Dogovorom je utvrđeno da se anoda piše sa leve, a katoda sa desne strane.
Rastvore polućelija je potrebno spojiti elektrolitičkim (sonim) mostom kako bi došlo do spontanog proticanja električne energije (spontanog kretanja elektrona sa anode na katodu).
Soni most je cevčica u obliku slova U u kojoj se nalazi koncentrovani rastvor nekog inertnog elektrolita koji ne reaguje sa komponentama polućelija a služi za održavanje električne ravnoteže u rastvorima koje povezuje.
Anoda predtavlja elektrodu na kojoj se odvija oksidacija:
Zn (s) ---> Zn2+ (aq) + 2e-
Katoda predstavlja elektrodu na kojoj se odvija redukcija:
Rastvore polućelija je potrebno spojiti elektrolitičkim (sonim) mostom kako bi došlo do spontanog proticanja električne energije (spontanog kretanja elektrona sa anode na katodu).
Soni most je cevčica u obliku slova U u kojoj se nalazi koncentrovani rastvor nekog inertnog elektrolita koji ne reaguje sa komponentama polućelija a služi za održavanje električne ravnoteže u rastvorima koje povezuje.
Elektrodni potencijal
Elektrodni potencijal je potencijal koji se uspostavlja između metala i jona u rastvoru i predstavlja tendenciju primanja ili otpuštanja elektrona.Anoda predtavlja elektrodu na kojoj se odvija oksidacija:
Zn (s) ---> Zn2+ (aq) + 2e-
Katoda predstavlja elektrodu na kojoj se odvija redukcija:
Cu 2+ (aq) + 2e-
---> Cu (s)
Standardna vodonična elektroda
Apsolutnu vrednost pojedinačnog elektrodnog potencijala nije moguće individualno (izolovano) izmeriti. Moguće je meriti razliku elektrodnih potencijala (tj. razliku potencijala polućelija). Kao elektroda za poređenje uzeta je standardna vodonična elektroda.
Standardna vodonična elektroda se sastoji od pločice platine obložene prahom platine (katalizator) uronjene u rastvor kiseline u kojoj je koncentracija H+ jona 1 mol/dm3i kroz koji prolazi gas H2 pod pritiskom od 1atm na temperaturi 25Co
1atm = 101325Pa
Standardni elektrodni potencijal
Standardni elektrodni potencijal (
Eo) je potencijal neke polućelije (elektrode) pri koncentraciji 1 mol/dm3 svih učesnika u elektrodnom procesu, za gasove pri pritisku od 1atm i na temperaturi od
25Co izmeren u odnosu na standardnu vodoničnu elekrtrodu.
Zahvaljujući uvođenju standardne vodonične elektrode određene su vrednosti za Eo za praktično sve moguće elektrohemijske reakcije:
Eoćelije =
Eokatode - Eoanode
Standardni elektrodni potencijal odgovara elektrohemijskoj reakciji redukcije tako da predstavlja standardni redukcioni potencijal.
Predznak minus (-) ili plus (+) određen je stvarnim predznakom, odnosno naelektrisanjem posmatrane elektrode koje ona ima kada je povezana (spregnuta) sa standardnom vodoničnom elektrodom u galvanskoj ćeliji.
Zn2+ + 2e-
---> Zn Eo (Zn/Zn2+) = -0.76V
Cu2+ + 2e-
---> Cu Eo (Cu/Cu2+) = +0.34V
Elektroda sa većom vrednošću je katoda.
Eoćelije =
Eo (Cu/Cu2+) - Eo (Zn/Zn2+)
Eoćelije =
0.34 - (-0.76)
Eoćelije
= 1.10V



Нема коментара:
Постави коментар